政策东风加速创新药械落地 从“港澳药械通”看第一类医疗器械的市场机遇
我国医药健康领域改革步伐不断加快,一系列旨在优化审评审批、加速创新产品上市的政策相继出台。其中,“真实世界数据”的应用与“港澳药械通”等政策的落地,正为医疗器械,尤其是第一类医疗器械的研发、获批与销售,注入强劲动力,开启了行业发展的新篇章。
政策组合拳:疏通药械上市“快车道”
1. 真实世界数据(RWD)的价值释放
传统医疗器械的临床试验往往周期长、成本高。而“真实世界数据”指在日常医疗实践中收集的与患者健康状况和/或诊疗及保健有关的数据。国家药监局已发布相关指导原则,鼓励将真实世界证据用于支持医疗器械的临床评价。对于部分第一类医疗器械(风险程度低,实行常规管理即可保证其安全、有效)而言,利用在临床使用中积累的真实世界数据来证明其安全有效性,可以简化临床评价要求,显著缩短产品上市前的验证周期,降低企业成本,使产品能更快地服务于临床需求。
2. “港澳药械通”政策的桥梁作用
“港澳药械通”政策允许在粤港澳大湾区内地指定的医疗机构,使用已在香港、澳门上市但未在内地注册的临床急需药品和医疗器械。这一政策具有双重加速效应:
- 先行先试,积累数据:国际先进的医疗器械可率先在指定医疗机构使用,其产生的临床使用数据和经验,可以作为该产品未来正式申请在内地上市的重要参考和证据,特别是宝贵的真实世界数据。
- 市场预热与渠道探索:对于有意进入内地市场的境外第一类医疗器械,该政策提供了一个低风险的市场切入点和渠道试水机会。通过早期在高端医疗机构的临床应用,可以建立品牌认知度,了解内地市场的实际需求与操作流程,为后续大规模市场推广铺平道路。
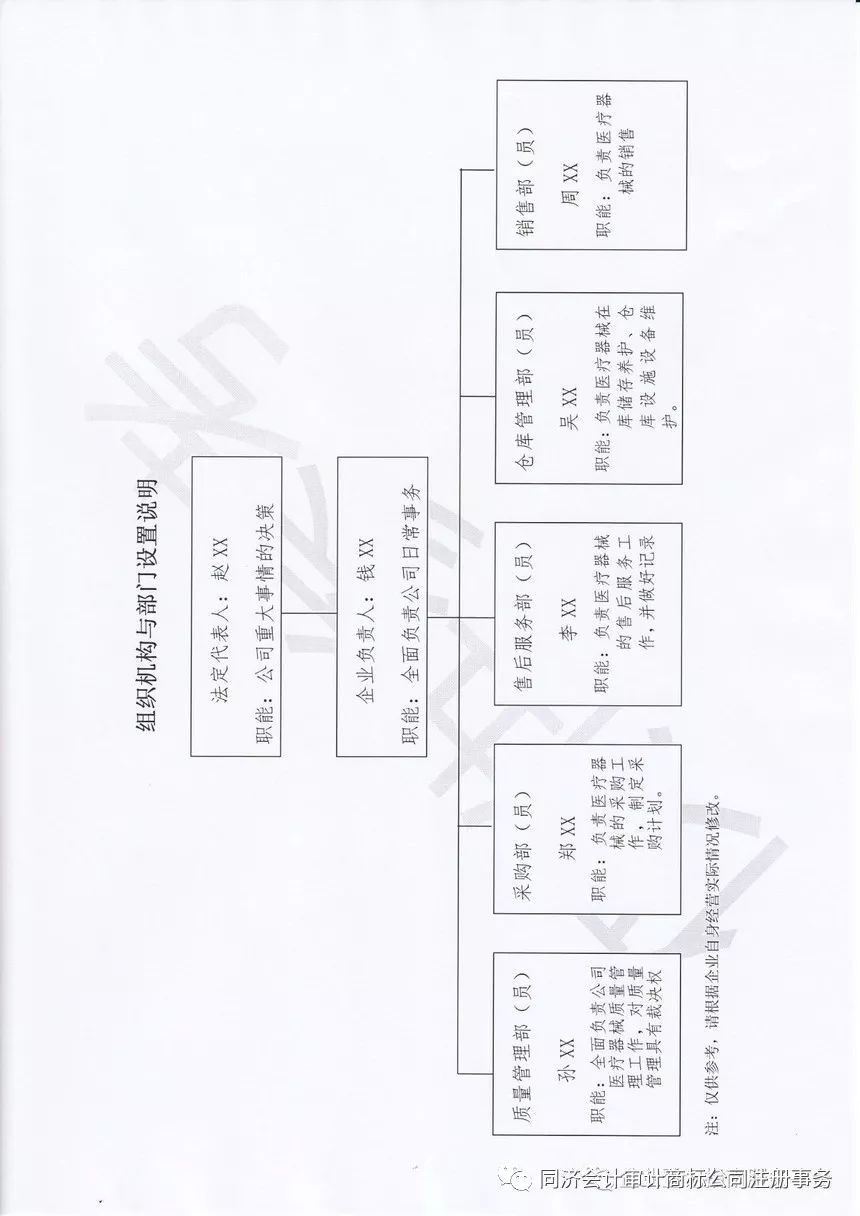
聚焦第一类医疗器械:在简政放权中抓住销售先机
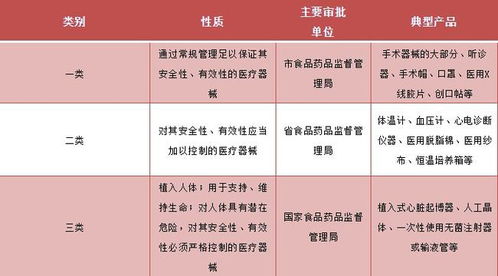
第一类医疗器械通常包括外科用器械、病房护理设备、部分物理治疗设备等基础型、低风险产品。在现行法规下,其备案管理流程已相对简化。而上述宏观政策的推进,进一步为其市场拓展创造了有利条件:
1. 上市路径更便捷:企业可以更灵活地运用真实世界证据支持备案,加速产品完成上市前合规步骤。对于已有港澳上市记录的产品,通过“药械通”通道积累的内地使用经验,能进一步增强其安全有效性说服力,简化注册备案材料。
2. 市场准入效率提升:政策整体营造了鼓励创新、快速响应的监管环境。医疗机构,尤其是大湾区内的机构,对新器械、新技术的接受度和试用意愿可能因政策引导而提高。这为第一类医疗器械的临床推广和销售提供了更友好的早期环境。
3. 销售策略的联动与创新:销售企业可以关注通过“港澳药械通”进入内地机构的器械名单,这些产品往往代表了一定的技术先进性和市场潜力。可以前瞻性地与相关生产企业建立联系,布局未来代理或销售合作。利用政策带来的市场关注度,加强自身对第一类器械的学术推广和专业服务能力,从单纯的渠道商向解决方案提供商转型。
展望与建议
“真实世界数据”应用与“港澳药械通”等政策,是深化医药卫生体制改革、满足人民群众健康需求的重要举措。它们不仅加速了高端创新药械的可及性,也为整个医疗器械产业链,包括看似“普通”的第一类医疗器械,带来了结构性的机遇。
对于医疗器械生产企业及销售商而言,应当:
- 深入研究政策细节,主动学习利用真实世界研究支持产品评价的方法。
- 关注粤港澳大湾区的动态,探索利用“药械通”等渠道进行产品先行布局的可能性。
- 强化产品全生命周期质量管理,即使对于备案管理的第一类器械,也需确保安全有效,积累良好数据与口碑。
- 创新商业模式,结合政策导向和临床实际需求,提供更具价值的产品与服务组合。
在政策东风的吹拂下,中国医疗器械市场正迎来一个更加开放、高效、以临床价值为导向的新阶段。准确把握政策脉搏,顺势而为,将是企业在竞争中脱颖而出的关键。
如若转载,请注明出处:http://www.tbsaasmall.com/product/24.html
更新时间:2026-04-22 14:33:57